Auf einen Blick
Inhaltsverzeichnis
Bezeichnung: Faktor V-Leiden-Genmutation
Ähnliche Tests:
Wann wird auf Faktor V Leiden untersucht?
Warum wird auf Faktor V Leiden / Prothrombinmutation untersucht?
Zur Bestimmung einer vererbten Genmutation, die das Risiko einer venösen Thrombembolie erhöht (VTE- eine unangemessene Blutgerinnselbildung, die den Blutfluss in den Venen unterbricht).
Bei welchen Erkrankungen sollte auf Faktor-V-Leiden / Prothrombinmutation untersucht werden?
Bei oder nach einer ungeklärten thrombotischen Episode, besonders bei relativ jungen Patienten (jünger als 50 Jahre) und bei Abwesenheit anderer thrombophiler Risikofaktoren.
Mit welchem Probenmaterial wird Faktor V Leiden / Prothrombinmutation durchgeführt?
Mit Blut aus einer Armvene.
Table of Contents
Das Probenmaterial
Was wird untersucht?
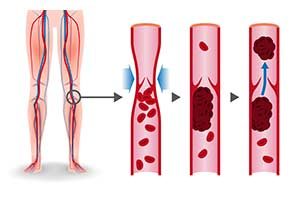
Faktor V und Prothrombin sind Gerinnungsfaktoren. Diese Proteine (Eiweiße) werden z. B. bei einer Gefäßverletzung Schritt für Schritt in der sogenannten Gerinnungskaskade aktiviert. Endpunkt der Gerinnungskaskade ist die Bildung eines Blutgerinnsels, das die verletzte Stelle des Gefäßes verschließt.
Faktor V Leiden ist eine Variante des Faktor V, das sich vom Faktor V durch einen Aminosäureaustausch unterscheidet. Grundlage dieses Unterschieds ist eine genetische Punktmutation – die Veränderung eines der Nukleotide auf dem Gen, das für die Herstellung des Faktor-V-Proteins codiert.
Dieses veränderte Protein hat eine normale Funktion in der Blutgerinnung; es wird aber bedeutend langsamer als der normale Faktor V durch das aktivierte Protein C (APC) während der Gerinnungskaskade wieder abgebaut.
Die Prothrombinmutation G20210A führt nicht zu einer veränderten Form des Prothrombinproteins, sondern die genetische Punktmutation liegt im Promoter des Gens und führt so zu einer erhöhten Synthese von Prothrombin und somit zu höheren Plasmaspiegeln an Prothrombin. Diese Mutation und die dadurch erhöhte Prothrombinmutation ist mit einem erhöhten Risiko für VTE verbunden.
Faktor V Leiden und Prothrombinmutation sind voneinander unabhängige Mutationen; die jeweilige Untersuchung dient dazu herauszufinden, ob eine der beiden Mutation vorliegt, der Betroffene hetero- oder homozygot für diese Mutation ist oder die normale Variante, den sogenannten Wildtyp, besitzt.
Wie wird das Probenmaterial für die Untersuchung gewonnen?
Aus Blut aus einer Armvene.
Faktor V Leiden Test
Wie wird der Test eingesetzt?
Untersuchungen des Fakor-V-Leiden und des Prothrombin G20210a werden in der Regel gemeinsam mit anderen Tests für die Hyperkoagulabilität angefordert, um bei der Diagnosestellung der Ursache von venösen Thromboembolien (VTE) zu helfen (als sogenannte Thrombophiliediagnostik).
Pixabay / frolicsomepl
Sie dienen der Suche nach dem Grund für die erste thrombotische Episode, besonders bei relativ jungen Patienten (unter 50 Jahren), wenn keine offensichtlichen auslösenden Faktoren bekannt sind (z. B. längere Bettruhe) oder die Thrombosen an einer ungewöhnlichen Stelle aufgetreten sind – wie an Venen der Eingeweide (mesenterial) oder des Gehirns (zerebral).
Auch bei der Untersuchung der Ursache von wiederholten Fehlgeburten kann die Untersuchung hilfreich sein. Als Ursache werden kleine Blutgerinnsel in den Gefäßen der Placenta vermutet.
Anstelle des direkten Nachweises des Faktor-V-Leiden wird teilweise auch eine funktionelle Untersuchung der aktivierten Protein-C (APC)-Resistenz eingesetzt. In etwa 95 % der Fälle von APC-Resistenz liegt auch eine Mutation des Faktor-V-Leiden vor; andere genetische Ursachen für eine APC-Resistenz sind bis zu 5 % verantwortlich.
Bei einer auffälligen APC-Resistenz sollte durch eine Bestimmung der Faktor-V-Leiden-Genmutation untersucht werden, ob der Betroffene für die Mutation homo- oder heterozygot ist. Davon abhängig ist die Dauer der Antikoagulation (Therapie mit blutverdünnenden Medikamenten). Bei Patienten unter Antikoagulation kann die APC-Resistenz nicht mehr zuverlässig bestimmt werden.
Die FII G20210A-Muatation muss immer durch einen Gentest diagnostiziert werden, der direkt nach dieser Muatation sucht. Dabei wird untersucht, ob der Patient für diese Veränderung homo- oder heterozygot ist. Die direkte Messung der Prothrombinspiegel wird nicht empfohlen, da sie nicht zuverlässig Personen mit der Mutation vom Wildtyp unterscheiden kann.
Risiken & Vorsorge
Wann sollte vorsorglich auch Faktor V Leiden untersiucht werden?
Bei Vorliegen dieser Mutation ist das Risiko erhöht, eine Thrombose zu entwickeln. Bei Bewertung der Ergebnisse ist aber zu beachten, dass das Thrombose-Risiko von einer Vielzahl von Faktoren reguliert wird. Diese Faktoren können die Thrombose fördern (Risikofaktoren) und aber auch davor schützen (protektive Faktoren). Deshalb erkranken viele Personen, obwohl sie die Mutation(en) besitzen, nicht an einer VTE.
Test – Wann sinnvoll?
Wann kann der Test sinnvoll sein?
Prothrombinmutation und Faktor-V-Leiden werden angefordert, wenn ein Patient seine erste venöse Thromboembolie (VTE) relativ jung (unter 50 Jahren) oder an ungewöhnlicher Stelle erleidet.
Auch wenn ein Patient eine persönliche oder familiäre Vorgeschichte von wiederkehrendem VTE aufweist, die erste VTE bei oraler Kontrazeption, Schwangerschaft oder Hormonersatztherapie erleidet, oder bei ungeklärten wiederholten Fehlgeburten ist eine Bestimmung zu erwägen.
Wenn bei einem Familienmitglied eine Faktor V Leiden- oder FII G20210A-Mutation bekannt ist, kann die Untersuchung sinnvoll sein. Eine noch asypmtomatische Person die weiß, dass sie an einer oder mehreren Mutationen leidet, kann andere kontrollierbare Gerinnungsrisikofaktoren wie orale Kontrazeption, Rauchen und die Hypercysteinämie beeinflussen und z.B. während Operationen oder längerer Mobilisation durch eine Antikoagulation sein Risiko senken.
Die genetischen Tests Faktor-V-Leiden-Mutation und FII G20210A-Mutation sollten nur einmal im Leben durchgeführt werden, da sie sich nicht verändern.
Das Testergebnis
Was bedeutet das Testergebnis?
pixabay/jochenpippir
In 95 % der Fälle ist eine APC-Resistenz auf Faktor V Leiden zurückzuführen. Beim Vorliegen der Resistenz sollte die Faktor-V-Leiden-Mutation durch einen Gentest bestätigt werden.
Faktor-V-Leiden ist die häufigste thrombophile Gerinnungsstörung. Die Prävalenz bei Menschen mit europäischer Abstammung liegt bei etwa 5 %. Ein Patient mit Faktor V Leiden kann heterozygot (er hat also eine Kopie des veränderten und eine des normalen Gens, als Wildtyp bezeichnet) oder homozygot (seltener, zwei Kopien des veränderten Gens) sein.
Die Heterozygoten haben ein etwa 5-10 % höheres Risiko, eine VTE zu entwickeln als die Normalbevölkerung; das Risiko bei den Homozygoten, irgendwann im Laufe des Lebens eine VTE zu entwickeln.
Das Vorliegen einer pt 20210-Mutation mit einer veränderten Genkopie bezeichnet man als heterozygot, das von zwei veränderten Kopien als homozygot. Die FII-G20210A-Mutation ist seltener als der Faktor-V-Leiden; man findet sie bei etwa 1-2 % der Bevölkerung.
Wissenswertes
Was sollte man außerdem wissen ?
Faktor-V-Leiden, Prothrombinmutation und die anderen erworbenen oder ererbten Mängel an thrombophilen Faktoren (Risiko, Blutgerinnsel zu entwickeln, Protein-C- und-S-Mangel) sind voneinander unabhängig. Man kann somit mehr als eine der Veränderungen tragen.
Die jeweiligen Risiken der thrombophilen Faktoren können sich addieren; bei einigen Formen ist die Kombination von zwei Faktoren erheblich ungünstiger als die beiden Faktoren allein (“potenziertes Risiko“).
Das pseudohomozygote Faktor V Leiden ist sehr selten. Es wird durch eine ererbte heterozygote Faktor-V-Leiden-Mutation und einen heterozygoten Faktor-V-Mangel hervorgerufen. Patienten mit diesen Mutationen haben verringerte Spiegel des normalen Faktor V und ein verändertes Faktor-V- Leiden-Protein (Eiweiß). Ihr Risiko für Thrombosen gleicht dem einer Person, die homozygot für eine Faktor-V-Leiden-Mutation ist.
Hinweise & Störungen
Stabilität und Probentransport
Die Untersuchungen auf Faktor-V-Leiden und die FII-G20210A-Mutation werden in der Regel mit EDTA-Blut durchgeführt. Zitratblut als Untersuchungsmaterial ist auch möglich; dagegen ist Heparinblut nicht geeignet. Proben können bei Raumtemperatur (Postversand) verschickt werden.
Störfaktoren und Hinweise auf Besonderheiten
Die molekulare Diagnostik ist auch bei oral antikoagulierten Patienten möglich. Die funktionelle Untersuchung (APC-Resistenz) kann durch Antikoagulantien gestört sein.
Richtlinien zur Qualitätskontrolle
Für den Nachweis der Faktor VLeiden-Genmutation und der Prothrombin G20210A-Genmutation besteht entsprechend der Richtlinien der Bundesärztekammer (RILIBÄK) keine Pflicht zur Teilnahme an externen Ringversuchen. Interne Kontrollen sowie die Bestimmung der Richtigkeit und Präzision müssen selbstverständlich regelmäßig durchgeführt werden. Die freiwillige Teilnahme an Ringversuchen ist möglich.
Häufige Fragen (FAQ)
Sollte jemand mit einer Faktor-V-Mutation auf eine Langzeitantikoagulation eingestellt werden?
Träger einer Faktor-V Leiden-Mutation haben nach einer ersten Thrombose ein sehr hohes Risiko, eine weitere Thrombose zu erleiden. In der Regel ist daher bei ihnen eine längere, unter Umständen mehrjährige Antikoagulation sinnvoll. Eine Antikoagulation von Patienten, die noch keine Thrombose erlitten haben, wird allgemein nur bei weiteren thrombophilen Risikofaktoren indiziert sein.
Wie wird eine tiefe Venenthrombose (VTE) behandelt?
Unabhängig von der zugrunde liegenden Ursache wird eine VTE immer mit einer kurzzeitigen Antikoagulation behandelt (meist drei bis sechs Monate mit einer Kombination aus Heparin und oralen Antikoagulantien wie Markumar). Am Ende dieses Zeitraumes wird anhand der vorhandenen Risikofaktoren überprüft, ob eine weitere Therapie notwendig ist.