Untersuchungsmethode der Nuklearmedizin
Flutemetamol (18F) PET-Tracer-Molekül zur Diagnose der Alzheimer–Krankheit.
Shutterstock / molekuul_be
Tracer werden besonders in der Nuklearmedizin mit Erfolg eingesetzt, wenn es darum geht, die Beschaffenheit und die Funktion eines Organs wie beispielsweise der Schilddrüse zu untersuchen.
Viele Untersuchungsmethoden verwenden diese Tracer, um bestimmte Organe zu Untersuchungszwecken und einer sicheren Diagnostizierung darzustellen.
Tracer werden in der Forschung, Biologie, Biochemie, Wasserwirtschaft für die Gewässerkartierung u. a. wissenschaftlichen Gebieten zu Untersuchungszwecken verwendet. In diesem Ratgeber informieren wir Sie umfassend zum Thema Tracer.
Table of Contents
Was ist ein Tracer?
Inhaltsverzeichnis
Die sogenannte Tracer-Methode hingegen beschäftigt sich eher mit Leitmerkmalen oder Kriterien von einer Abfolge bestimmter Behandlungsmethoden.
Typische Tracerdiagnosen im Sinne von Qualitätsmerkmalen sind für Diagnostik, OP-Verfahren, OP-Befunde, Risikofaktoren, Intra-OP-Diagnostik und Komplikationen in der Literatur nachzulesen.
Die Einsatzbereiche dieser Tracer-Methoden behandeln dabei das Management-System beim Myocardinfarkt, Pneumonien, Antibiotika-Therapien, Dekubitusprophylaxe oder Eigenblut- und Fremdblutgabe u. a.
Der Tracerbegriff an sich wird hauptsächlich der Nuklearmedizin zugeordnet. Die Tracer sind körpereigene oder körperfremde Stoffe mit einer radioaktiven Imprägnierung.
Durch die Teilnahme dieser Tracer, am Stoffwechselprozess des Körpers werden Spuren im Körper gesetzt, die eine Untersuchung des Organs durch den Arzt oder Radiologen ermöglicht.
Chemische Elemente besitzen gleiche Protonen- und Elektronenzahl. Ist die Protonenzahl zur Neutronenzahl verschieden, nennt man diese Atome Nuklide und speziell Isotope. Atome mit hoher Ordnungszahl können sich verändern, sind also instabil.
Durch die Veränderung entstehen Strahlungen, die als Radioaktivität bezeichnet wird. Dabei werden Alpha-Strahlen (Helium-Kerne), Beta-Strahlen (Elektronen) und Gamma-Strahlen (elektromagnetische Wellen) freigesetzt.
Radioaktive Isotope
Welche radioaktiven Isotope finden in der Medizin Verwendung?
| Isotop | Halbwertzeit | Strahlung | Anwendung |
| H-3 (Tritium) | 12,3 Jahre | Beta | Forschung: Tracer |
| C-14 (Kohlenstoff) | 5568 Jahre | Beta | Forschung: Tracer, Altersbestimmung |
| P-32 (Phosphor) | 14,4 Tage | Beta | Forschung: Tracer, Strahlentherapie (Knochen) |
| S-35 (Schwefel) | 87 Tage | Beta | Forschung: Tracer, Tumordiagnostik |
| Co-57 + Co-58 (Cobalt) | 270 / 71 Tage | Beta, Gamma | Diagnostik: Schilling-Test |
| Co-60 | 6,2 Jahre | Beta, Gamma | Strahlentherapie (extern) |
| Tc-99m (Technitium) | 6 Stunden | Gamma | Diagnostik: Szintigrafie |
| Cs-137 (Cäsium) | 30 Jahre | Beta | Strahlentherapie (extern) |
| I-123 (Jod) | 13 Stunden | Gamma | Diagnostik: Szintigrafie |
| I-131 | 8,4 Tage | Beta, Gamma | Radiojodtest, Radiojodtherapie |
| Ir-192 (Iridium) | 74 Tage | Beta | intrakavitäre Strahlentherapie |
| Au-198 (Gold) | 2,7 Tage | Beta | interstitielle Strahlentherapie |
| Rn-222 (Radon) | 3,8 Tage | Alpha | Kur-Zwecke (Radonquellen) |
| Ra-226 (Radium) | 1622 Jahre | Alpha | Strahlentherapie (intern) |
| U-238 (Uran) | 8,4 Tage | Alpha (Beta, Gamma) | Herstellen von Transuranen |
Ursprung & Entwicklung
1949 beschrieb erstmals die Berechnung der Gewebedurchblutung aus der Zeitkonstante des Aktivitätsabfalls eines radioaktiven Natriums (Clearance, Auswaschvorgang). Diese Methode wurde später weiterentwickelt. Andere nuklearmedizinische Tracer wurden modifiziert, wobei besonders unter Daly und Henry 1980, Lassen 1964 und Sejrsen 1971) dem Xe (Xenon) eine wesentliche Bedeutung zukam.
Die Isotopen-Clearance diente vor allem zu Messung der Haut– und Muskeldurchblutung. Bereits zu diesem Zeitpunkt von Larsen 1966, Lassen 1964 und Sejrsen 1971 konnte der radioaktive Tracer intramuskulär sowie epi-, intra- und subkutan appliziert werden.
Funktion, Wirkung & Ziele
Wie in der Tabelle zu ersehen ist, werden die verschiedensten Isotope sowohl in Behandlungen und Therapien als auch in der Diagnose eingesetzt. In Behandlungen, Therapien und Diagnosen kommen größtenteils die Isotope mit der geringsten Halbwertszeit zur Anwendung.
Diese sind in folgende Behandlungsformen vertreten:
- Strahlentherapie (extern, intern)
- intrakavitäre Strahlentherapie
- interstitielle Strahlentherapie
- metabolische Strahlentherapie
- Radiojodtest, Radiojodtherapie
- Radonquellen zu Kur-Zwecken
- Forschungszwecke (C14 – Methode zur Altersbestimmung von biologischen Substanzen)
Ablauf & Wirkungsweise
Durchführung und Funktionsweise
Die Durchführung und Wirkungsweise unterscheiden sich je nach Art der Therapie bzw. Diagnose. Daher werden diese nachfolgend im Einzelnen erläutert.
Strahlentherapie
Die Strahlentherapie wird fast ausschließlich in der Tumorbehandlung maligner Neoplasien verwendet. Diese Behandlungsform wird oft mit chirurgischen und chemotherapeutischen Maßnahmen kombiniert. Man unterscheidet zwischen externer Strahlentherapie, metabolischer Strahlentherapie und interner Strahlentherapie.

Strahlentherapie
Die interne Strahlentherapie
Die interne Strahlentherapie unterteilt sich wiederum in interstitielle und intrakavitäre Strahlentherapie. Die interstitielle Strahlentherapie findet ihren Einsatz bei nicht operablen Bronchialkarzinomen. Mittels radionuklidhaltiger Nadeln wird mit 198-Au in das Tumorgewebe appliziert.
Man nennt diese Methode auch die Spickmethode. Bei der intrakavitären Strahlenmethode werden verkapselte Radionuklide in Organhöhlen appliziert. Zum Teil sind diese noch leer und werden erst dann mit einer radioaktiven Substanz gefüllt. Anwendung findet sie vor allem in Rektum Nase, Mund, Uterus, Vagina, Zervix und Ösophagus.
Die metabolische Strahlentherapie
Bei der metabolischen Strahlentherapie wird bei bestimmten Tumoren Radionuklid injiziert, das an Trägermoleküle gebunden ist, die sich dann im Tumor konzentrieren.
Die externe Strahlentherapie
Bei der externen Strahlentherapie kommen vorwiegend Gammastrahlen (60-Co) oder ultraharte Röntgenstrahlen zum Einsatz. Ziel ist immer die maximale Schädigung des Tumorgewebes mit geringster Beeinträchtigung des umliegenden gesunden Gewebes. Deshalb wird die Strahlung mit einer Bestrahlungs-Geometrie beweglicher Strahlenquellen durchgeführt und die Eindringtiefe auf den Tumor fokussiert.
Radiojodtherapie
Diese Therapie kommt bei bestimmten Formen des Schilddrüsenkarzinoms, bei Hyperthyreose oder Struma Basedow und bei nichtoperablen Patienten zum Einsatz. Dabei werden höhere Dosen von 131-I zugeführt. Diese Substanz lagert sich in die Schilddrüse ein und zerstört das erkrankte Gewebe.
Diese Behandlung wird in isolierten Zimmern bzw. Stationen eines Krankenhauses durchgeführt und die Patienten müssen wegen der höheren Strahlung in dieser Zeit isoliert im Krankenhaus verbleiben. Auch die sogenannten heißen Knoten können damit erfolgreich behandelt werden.
In der Forschung
Tracer in der Forschung dienen der Aufklärung von Stoffwechselwegen und Wirkungsmechanismen. Dafür werden Wirkstoffe markiert und deren Verbleib und Abbau im Organismus untersucht und nachgewiesen.
Die Radiokarbonmethode
C14-Analyse (Radiokarbonmethode) zur Altersbestimmung: Hier handelt es sich um ein Verfahren radiometrischer Datierung von organischen, kohlenstoffhaltigen Materialien. Das Verfahren beruht auf der Kenntnis, dass in abgestorbenen Organismen die radioaktiven 14-C Atome nach dem Zerfallsgesetz Abnehmen. Lebende Organismen bilden ständig durch die Aufnahme von Kohlenstoff den normalen Anteil von 14-C-Atomen neu.
Hilft gegen
Wogegen hilft eine Tracer-Strahlentherapie?
- Bronchialkarzinome
- Schilddrüsenkarzinom
- Hyperthyreose
- Struma Basedow u. a.
Sowie bei folgenden Tumoren und Karzinomen:
Diese genannten Anwendungsgebiete u. a. werden vorwiegend erfolgreich mit der Strahlentherapie behandelt.
Fördert & stärkt
Durch diese Behandlungsformen in Kombination mit operativen und chemotherapeutischen Maßnahmen wird das kranke Gewebe entfernt. Ziel dabei ist es, das gesunde Gewebe zu schonen, damit die behandelten Organe wieder zu einer normalen Funktionsweise zurückkehren. Normal funktionierende Organe stärken selbstverständlich die Patientengesundheit und retten oft Leben. Durch eine anschließende medikamentöse Therapie wird größtenteils der normale Level wiederhergestellt.
Diagnose & Untersuchung
Diagnostik und Untersuchungsmethoden
Als Tracer-Diagnoseverfahren sind folgende in Anwendung:
- Strahlentherapie in der Tumordiagnostik
- Szintigrafie
- Positronen-Emissions-Tomografie (PET)
- SPECT
- Schilling-Test
- Radiojodtest
Strahlentherapie in der Tumordiagnostik: s. o.
Voraussetzung für eine erfolgreiche Therapie ist die vollständige Erfassung der Tumormasse. Dazu wird heute die Computertomografie nach einer Bildfusion mit MR oder PET-Daten ein dreidimensionales Bild dargestellt und ein geeigneter Strahlentherapieplan festgelegt. Mittels der Radiochemotherapie, der Radiochirurgie, der Radiojodtherapie, der Radionuklidtherapie bzw. einer Radioimmuntherapie kann der Tumor behandelt werden.
Szintigrafie
Szintigrafie ist ein nuklearmedizinisches Verfahren, das Körpergewebe sichtbar darstellt. Dafür werden schwach radioaktive Stoffe (Tracer) verabreicht, die sich in den Organen ansammeln.
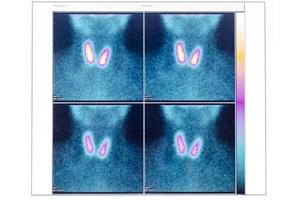
Szintigraphie der Schilddrüse
Shutterstock / Stefania Arca
Die abgegebene Strahlung wird gemessen und kennzeichnet die Stoffwechselaktivität und die Durchblutung des Gewebes. Bei der Schilddrüsenszintigrafie wird radioaktives Jod injiziert, bei anderen Fällen wird die radioaktive Substanz an Eiweiße oder Salze gebunden, die von bestimmten Organen verstoffwechselt werden.
Das Radiopharmakon zerfällt und gibt Gammastrahlen ab, die mit einer speziellen Gammakamera gemessen wird. Am Computer wird dann das Bild (Szintigramm) erstellt. Verstärkte Stoffwechselaktivitäten finden sich besonders bei Entzündungen und Tumoren. Verminderte Aktivitäten können auf abgestorbenes Gewebe verweisen. Mithilfe der Szintigrafie können die verschiedensten Gewebe untersucht werden. Zum Beispiel gibt es die:
Knochen
Knochenszintigrafie
Der Verlauf erfolgt wie bereits geschildert. Als radioaktive Markierung werden mit Technetium (99m Tc) markierte Phosphonate verwendet. Je nach Bedarf kann man eine Teilkörperskelettszintigrafie oder eine Ganzkörperszintigrafie durchführen, um eventuelle Metastasen zu diagnostizieren. Bei der Mehrphasenszintigrafie (3-Phasen-Skelettszintigrafie) werden zu unterschiedlichen Zeitpunkten Aufnahmen gemacht.
Durch die Darstellung des Blutflusses in Venen und Arterien können Entzündungen oder Knochen-Metastasen diagnostiziert und beurteilt werden. Die Knochenszintigrafie wird eingesetzt bei Knochenkrebs, Knochenmetastasen, Knochenentzündung (Spondylodiszitis, Osteomyelitis), rheumatoide Arthritis (Rheuma), Knocheninfarkt und Störungen des Knochenstoffwechsels wie bei Osteomalazie oder Morbus Paget.
Schilddrüse
Schilddrüsenszintigrafie
Bei der Schilddrüsenszintigrafie injiziert man das radioaktive Technetium-Pertechnetat oder Natriumchlorid in die Vene. Bei der MIBI-Szintigrafie und mIBG-Szintigrafie bekommt der Patient mit techneticum-markiertes Methoxy-Isobutyl-Isonitril in die Vene verabreicht, wodurch besonders kalte Schilddrüsenknoten abgeklärt werden können. Kalte Knoten können bösartig sein. Bei der mIBG-Szintigrafie wird Meta-Iodobenzylguanidine radioaktiv markiert und dem Patient intravenös verabreicht.
Diese Untersuchung dient ebenfalls der Diagnose möglicher Krebstumoren. Mit der Suppressionsszintigrafie können autonome Schilddrüsenareale besser abgeklärt werden, die unabhängig vom Gehirn Schilddrüsenhormone produzieren. Die Vorbereitung beginnt mehrere Tage vorher mit der Einnahme hoch dosierter Schilddrüsenhormone. Dadurch wird die Aktivität gedrosselt (supprimiert).
Die nachfolgende Szintigrafie erfolgt mit der Gabe von Technetium-Pertechnetat, das die nicht gedrosselten Areale anzeigt. Kalte Knoten speichern wenig oder kein Radiopharmakon, was Anzeige für einen bösartigen Tumor sein kann. Ein warmer Knoten speichert das Mittel etwas stärker. Dabei handelt es sich oft um gutartige Tumore. Heiße Knoten speichern das Mittel sehr intensiv. Es handelt sich um einen gutartigen Knoten, der völlig unabhängig Schilddrüsenhormone produziert.
Myocard
Myocardszintigrafie
Mit dieser Untersuchungsform wird die Durchblutung des Herzmuskels dargestellt. Für die radioaktive Markierung wird meist Technetium-99m (99mTc) als Radiopharmakon verwendet. Die Myocardszintigrafie kann in Ruhe oder unter Belastung durchgeführt werden. Man kann auch vorsichtig mittels Medikamenten wie Adenosin oder Vasodilatatoren eine vorsichtige Belastung initiieren.
Bei einem schlecht durchblutenden Herzmuskel erscheint weniger Strahlung. Bei verminderter Anreicherung gibt es 2 Unterschiede, zum einen tritt die verminderte Anreicherung nur unter Belastung auf oder zum anderen unter Belastung und im Ruhezustand. Beim Ersten handelt es sich um einer reversible Perfusionsstörung, beim Zweiten um eine nicht-reversible Perfusionsstörung. Der betroffene Herzmuskelbereich ist dann irreversibel zerstört. Stenosen von Herzkranzgefäßen können mit einer Myocardszintigrafie nicht lokalisiert werden.
Man führt diese Untersuchung durch bei Verdacht auf eine koronare Herzerkrankung. Auch nach einem Herzinfarkt kann der Zustand des Herzmuskels besser beurteilt werden. Die Patienten müssen zu dieser Untersuchung mit Ausnahme von Diabetikern nüchtern erscheinen. Ist der Einsatz von Vasodilatatoren geplant, dürfen 12 Stunden vor der Untersuchung keine koffeinhaltigen Speisen oder Getränke verkonsumiert werden. Bestimmte Medikamente mit Koffein müssen 24 Stunden vorher abgesetzt werden.
Nieren
Nierenfunktionsszintigraphie:
Diese Untersuchungsmethode basiert auf Messung von radioaktiv markierten Flüssigkeiten im Organismus. Der Tracer wird intravenös appliziert. Der Patient bekommt zu diesem Zweck intravenös sowohl in den linken als auch in den rechten Arm einen venösen Zugang in Form eines Schlauches gelegt. Der zweite Zugang dient nach Beendigung der Untersuchung der Blutentnahme.
Mitunter erhält der Patient nach der Verabreichung des radioaktiven Materials ein Diuretikum, das die Harnproduktion anregen soll. Der Patient hat den Rücken liegend oder sitzend der Gammakamera zugewandt. Die Untersuchung dauert ungefähr 20 bis 30 Minuten. Als Vorbereitung der Untersuchung muss der Patient vorher viel trinken. Die Strahlenbelastung ist gering.
Octreotid
Somatostatin-Rezeptor-Szintigrafie (Octreotid-Szintigrafie)
Bestimmte Tumore sind in normalen Verfahren (Röntgen, Ultraschall, CT, MRT) kaum diagnostizierbar. Diese neurendokrinen Tumore (NET) befinden sich häufig im Bauchraum (Pankreas, Magen, Darm). Sie produzieren Hormone. Auf der Oberfläche dieser Hormone kann das Hormon Somastatin andocken. Die Tumore können nun durch die Bindung des radioaktiven Octreotids an das Somastatin sichtbar gemacht werden.
PET
Positronen-Emissions-Tomographie (PET):
Wie bei der Szintigrafie wird dem Patient vor der Untersuchung ein Radiopharmakon verabreicht. Bei der PET werden Radionuklide verwendet, die Positronen (Beta-Plus-Strahlung) aussenden. Das PET-Gerät enthält ringförmige Detektoren für die Photonen, die um den Patient angeordnet sind.
Aus der räumlichen und zeitlichen Verteilung der Zerfallsereignisse kann auf die Verteilung des Radiopharmakons im menschlichen Organismus geschlossen werden. Bei der PET werden vorwiegend Isotope der Elemente Kohlenstoff, Stickstoff, Sauerstoff, Rubidium und Gallium eingesetzt.
| Nuklid | Halbwertzeit |
| 11-C, Kohlenstoff | 20,3 Minuten |
| 13-N, Stickstoff | 10,1 Minuten |
| 15-O, Sauerstoff | 2,03 Minuten |
| 18-F, Fluor | 110 Minuten |
| 68-Ga, Gallium | 68 Minuten |
| 82-RB, Rubidium | 75 Sekunden |
Anwendungsgebiete
Typische Anwendungsgebiete bestimmter Radiopharmaka sind hierbei:
| Nuklid | Radiopharmakon | Anwendungsgebiet/Sichtbarmachung/Darstellung |
| 11-C | 11-C-Cholin | Prostatakrebsdiagnose |
| 11-C-Pittsburgh compound | Alzheimer Frühdiagnose | |
| 11-C-S-Methyl-L-Methionin | Visualisierung: Proteinbiosynthese, Diagnose maligner Gliome | |
| 11-C-Azetat | Visualisierung: Stoffwechselverbrauch des Herzmuskels | |
| 13-N | 13-N-L-Glutaminsäure | Darstellung: Aminosäurestoffwechsel |
| 13-N-Ammoniak | Darstellung: Herzmuskeldurchblutung | |
| 15-O | 15-O-Wasser | Darstellung: Durchblutung (Perfusion) |
| 15-O-2 | Darstellung: Sauerstoffaufnahme und Verteilung | |
| 18-F | 18-F-Cholin | Prostatakrebsdiagnostik |
| 18-F-Floururacil | Darstellung: Tumore + Therapiekontrolle | |
| 18-F-Fluorethyltyrosin | Darstellung: Hirn-Tumore | |
| 18-F-Natriumfluorid | Darstellung: Knochenstoffwechsel | |
| 18-F-2-Flour-2-desoxy-D-glukose | Darstellung: Glucosetransport, Glucoseumsatz | |
| 18-F—6-Fluoro-DOPA | Darstellung: Diagnostik neuroendokriner Tumore | |
| 18-F-Florbetaben,-Florbetapir-,Flutemetamol | Alzheimer Früherkennung | |
| 68-Ga | DOTATOC | Somatostatin-Rezeptorbildumgebung neuroendokriner Tumore: Pankreastumor, Meningiom, Bronchialkarzinom, Karzinoid |
| PSMA | Prostatakrebsdiagnostik | |
| 82-RB | 82-RB-Chlorid | Darstellung: Herzmuskeldurchblutung |
SPECT und SPECT /CT
SPECT heißt Single Photon Emission Computed Tomography und ist eine Weiterentwicklung von mehreren Gamma-Kameras, die sich um den Patienten bewegen. Sie können dreidimensionale Schnittbilder erzeugen im Unterschied zur normalen Szintigrafie.
Schilling-Test: Vitamin B12-Resorption
Bei der Schilling-Methode werden Störungen bei der Aufnahme von Vitamin b12 untersucht. Der Patient erhält oral 1 Mikrogramm radioaktives 57-Co, wobei die Urinausscheidung 24 Stunden kontrolliert wird. Ein gesunder Patient scheidet mindestens 5 % des radioaktiv markierten Vitamin B12 aus. Gestörte Transportfunktionen können auf Darmepithelien oder Schleimhautödeme hinweisen. Auch Morbus Crohn ist mit dieser Methode erkennbar.
Radiojodtest:
Der Patient erhält oral 131-I-haltiges Präparat. Danach werden der Anstieg und der Abfall der Jodaktivität im Serum gemessen. Dieser Test wird aufgrund der hohen Strahlenbelastung nur noch als vorbereitende Medikation für eine nachfolgende Radiojodtherapie eingesetzt.
Risiken & Nebenwirkungen
Für den menschlichen Organismus besteht weder in der internen oder metabolischen Strahlentherapie noch in der PET-Untersuchung oder Szintigrafie durch die Vergabe von Tracern ein Risiko oder eine Belastung des Allgemeinzustandes. Der Patient scheidet nach kurzer Zeit die Tracer über den Urin aus. Die Strahlung, die von den Tracern ausgeht, kann mit einer natürlichen Radioaktivität verglichen werden. Bei einer Myocardszintigrafie dürfen bei Asthma oder niedrigen Blutdruck keine Medikamente wie Adenosin verwendet werden, es kann alternativ auf Katacholamin Dobutamin als Infusion zurückgegriffen werden.
Die Belastung auf dem Fahrradergometer bei einer Myocardszintigrafie kann zu Herzrhythmusstörungen und Herzinfarkt führen. Eine medikamentöse Belastung führt bei einer Myocardszintigrafie unter Umständen zu Brustschmerz, Atemnot, Blutdruckabfall, Herzrhythmusstörungen oder Herzinfarkt.
Gegenanzeigen
Denkbar ist eine Medikamentenunverträglichkeit gegen die Tracer, die eventuell Allergien auslösen können. Daher befragt der Arzt vor Behandlungen die Krankenanamnese ab. Allerdings darf in der Schwangerschaft und Stillzeit keine Schilddrüsenszintigrafie durchgeführt werden, da das werdende Kind Schaden nehmen könnte.